July 15, 2025
昌郁醫藥與神基製藥就鎮痛新藥XG005達成中國獨家授權合作

December 12, 2024
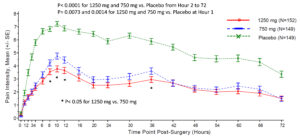
昌郁醫藥宣佈XG005片劑在美國術後疼痛的臨床2b/3期試驗中取得顯著陽性結果

October 25, 2024
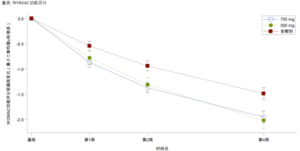
昌郁醫藥骨關節炎臨床研究結果被美國風濕病學會(ACR)2024年度大會作為最新摘要接收

August 08, 2024
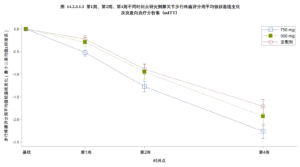
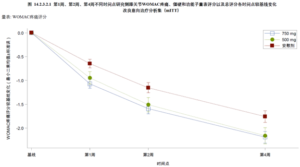
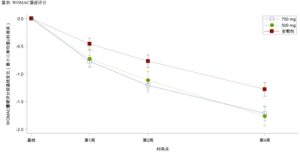
昌郁醫藥宣佈用於治療骨關節炎疼痛的創新藥XG005片劑在2b期臨床試驗中取得了顯著陽性結果

May 08, 2024
昌郁醫藥選擇性TRPM8受體拮抗劑XG2002膠囊I期臨床研究首組受試者入組完成

April 08, 2024
昌郁醫藥宣佈XG005中國膝骨關節炎II期臨床試驗完成目標受試者入組

March 11, 2024
昌郁醫藥創新鎮痛產品XG2002 臨床試驗獲得澳洲HREC批准

December 20, 2023
昌郁醫藥全新靶點鎮痛產品XG2002澳洲I期臨床研究正式啟動

August 23, 2023
昌郁醫藥宣佈XG005鎮痛在研產品完成在美國的手術後疼痛臨床2b/3期試驗首例患者入組

April 26, 2023
昌郁醫藥宣佈XG004外用透膚凝膠治療膝骨關節炎(OA)疼痛的1b/2a臨床試驗獲得陽性結果

December 22, 2022
昌郁醫藥首席醫務長姜廣良博士參加歐洲疼痛臨床試驗大會並做主題演講

December 13, 2022
昌郁醫藥宣佈XG005中國II期臨床試驗完成首例患者入組

November 21, 2022
昌郁醫藥姜廣良博士參加世界疼痛醫學大會

July 26, 2022
昌郁醫藥創新鎮痛產品XG004外用透膚凝膠正式啓動澳洲1b/2a期臨床試驗

March 04, 2022
世界知名的疼痛領域創新藥研發專家鄭國柱博士加入昌郁醫藥任職藥物研發長兼資深副總經理(CDO)

November 04, 2021
昌郁醫藥完成4000萬美元C輪超額融資,加速疼痛和神經產品線佈局

October 04, 2021
姜廣良博士加入昌郁醫藥任職醫務長(CMO)

September 29,2021
昌郁醫藥創新鎮痛產品XG005 I 期臨床橋接試驗啟動會正式舉行

September 22,2021
全球獨家!昌郁醫藥與RaQualia Pharma就全新鎮痛產品簽署授權協定

April 22,2020
XG005新藥上巿的申請,遵循 505(b)(1)法規的監管

May 4, 2019
昌郁醫藥公司完成B+輪融資

October 25, 2018
昌郁醫藥公司完成兩千萬美元B輪融資